昨天����,我根據(jù)一個網(wǎng)絡(luò)視頻寫了 “餓得死”的癌細胞 一文���,借助微信傳播和網(wǎng)站轉(zhuǎn)載��,“流毒”甚廣����,一時間弄得“謠言”滿天飛!有人質(zhì)疑�,生酮飲食真的可以把癌細胞餓死嗎?那個視頻并非嚴格的科學(xué)報道����,何足為憑?那些說法有沒有嚴格的科學(xué)論證���?
“餓得死”的癌細胞 一文���,借助微信傳播和網(wǎng)站轉(zhuǎn)載��,“流毒”甚廣����,一時間弄得“謠言”滿天飛!有人質(zhì)疑�,生酮飲食真的可以把癌細胞餓死嗎?那個視頻并非嚴格的科學(xué)報道����,何足為憑?那些說法有沒有嚴格的科學(xué)論證���?
生酮飲食“餓死”癌細胞的實驗源于何時���?
現(xiàn)在我恰好準備寫一篇有關(guān)胰島素及葡萄糖影響垂體瘤細胞生長的論文,于是帶著以上質(zhì)疑檢索了部分研究文獻���,尤其關(guān)注人類腫瘤的臨床試驗部分的實驗結(jié)果��。不查不知道�����,一查嚇一跳�����!原來早在1995年(也就是20年前)美國科學(xué)家就開展了生酮飲食治療兒童腦腫瘤的臨床試驗���。
在經(jīng)過短短7天的生酮飲食試驗后,兩例腦腫瘤女童患者的血糖比正常水平低��,而血中酮體水平升高20-30倍���,腫瘤部位的葡萄糖吸收平均降低了21.8%����。其中一名患者又追加了12個月的生酮飲食試驗�,結(jié)果未發(fā)現(xiàn)腫瘤進展的跡象(參考文獻1)。

生酮飲食抗腫瘤的動物實驗結(jié)果如何�����?
從1995年到2010年�����,在腦腫瘤動物模型中開展了大量生酮飲食與腦腫瘤生長相關(guān)性的研究�����,得出的結(jié)論都是生酮飲食可以抑制腦腫瘤生長,而且做出了非常樂觀的預(yù)期:生酮飲食是“有效治療惡性腦腫瘤的替代方法”(an effective alternative therapy for malignant brain tumor)(參考文獻2)����。

生酮飲食或配合放化療能治療人體腫瘤嗎?
到了2010年��,意大利科學(xué)家又在人體試驗中用生酮飲食(脂肪:碳水化合物+蛋白質(zhì)=4:1�,每日600千卡)治療多形性膠質(zhì)母細胞瘤(GBM)。經(jīng)過兩個月治療后�����,患者體重減輕20%����,而且腦中無可見腫瘤組織?��?墒?��,在停止治療后10周內(nèi),腫瘤就復(fù)發(fā)了(參考文獻3)����。

2014年���,美國匹茲堡大學(xué)癌癥研究所的研究人員配合放療、化療開展生酮飲食治療多形性膠質(zhì)母細胞瘤臨床試驗���,結(jié)果在6名參加生酮飲食療法的患者中,有4人在14個月的隨訪中全部存活下來(參考文獻4)�����。
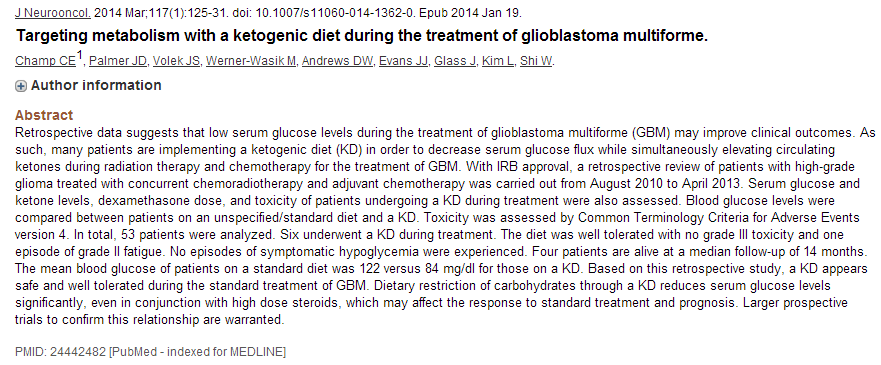
生酮飲食是否只對腦腫瘤有效���?
大家注意到���,以往開展的生酮飲食抗腫瘤的臨床試驗都是針對腦腫瘤的,莫非該療法對其他腫瘤無效����?還是讓數(shù)據(jù)來說話吧!在人乳腺癌��、胰腺癌和前列腺癌細胞移植腫瘤動物模型中�,生酮飲食是有明確治療效果的(參考文獻5、6�、7)�。顯然�����,生酮飲食對腦腫瘤以外的其他腫瘤的治療效果�,還有賴今后開展人體試驗進行驗證。
生酮飲食抗癌療法有無大型臨床試驗數(shù)據(jù)支持�?
迄今在美國NIH掛上號并已完成I期臨床試驗的是德國圖平根大學(xué)開展的復(fù)發(fā)性膠質(zhì)母細胞瘤研究(Ketogenic diet for Recurrent Glioblastoma,ERGO)�,從2007年開始,2010年結(jié)束�����,歷時3年(有圖為證���,原文網(wǎng)址:https://clinicaltrials.gov/show/NCT00575146)���。

在項目完成后,他們于2014年在《國際腫瘤學(xué)雜志》(Int J Oncol)發(fā)表文章��,全面總結(jié)了以上臨床試驗結(jié)果(參考文獻8)����。在總共20名參加臨床試驗的患者中����,他們得出如下幾個結(jié)論:
1�����、3位患者(15%)因無法耐受生酮飲食而放棄�����;
2���、未觀察到生酮飲食引起的嚴重副作用;
3��、接受測試的13位患者中有12位(92%)至少一次尿檢酮體陽性����;
4、1位患者稍有起色�,2位患者6周后病情穩(wěn)定;
5����、所有患者的平均無腫瘤進展存活期(PFS)為5周����,最短3周���,最長13周����;
6�����、平均存活期從試驗開始至32周���;
7�����、7位接受貝伐珠單抗與生酮飲食聯(lián)合治療的患者中有6位(86%)表現(xiàn)全部或部分客觀反應(yīng)���。

由于I期臨床試驗的主要目的是觀察人體對新藥的耐受程度,以便為制定給藥方案提供依據(jù)��,也就意味著該試驗的生酮飲食的配方及食用方法并非最佳,最終導(dǎo)致17位接受生酮飲食治療的患者出現(xiàn)病情進展�����。
在這些腫瘤復(fù)發(fā)患者中����,13位未實施拯救方案,8位接受藥物拯救治療����,并繼續(xù)輔以生酮飲食,其中1位用ACNU/teniposide����,4位用貝伐珠單抗���,3位用貝伐珠單抗和irinotecan���。用貝伐珠單抗者的平均PFS為21.1周(12-124周),達到6個月PFS的人數(shù)為43%�。
胰島素如何促進腫瘤生長?
一種被稱為萊昂綜合征(Laron's syndrome)的遺傳性侏儒癥�,源于生長激素受體基因缺陷。有趣的是����,這些病人患癌癥及糖尿病的風(fēng)險極低�����,推測生長激素與胰島素樣生長因子可能促進腫瘤增殖���。同時也發(fā)現(xiàn),胰島素及胰島素生長因子可以通過活化PI3K信號轉(zhuǎn)導(dǎo)通路促進葡萄糖向細胞內(nèi)的運輸����,而此過程受腫瘤抑制因子PTEN拮抗。
當(dāng)PTEN突變導(dǎo)致PI3K過度激活時��,細胞就傾向于攝入大量葡萄糖用于無氧呼吸(瓦勃效應(yīng))��,使代謝活性增高10-20倍��,結(jié)果產(chǎn)生過量活性氧自由基��,致使DNA損傷加劇�����,從而引起高頻率的細胞癌變。還發(fā)現(xiàn)糖尿病治療藥物二甲雙胍(甲福明)可使癌癥發(fā)生率降低25%-40%��,其間胰島素水平顯著降低��,推測高水平胰島素增大致癌風(fēng)險��。
在攝入高脂低糖的生酮飲食時�,由于血糖水平降低,胰島素分泌隨之減少���,于是將胰島素致癌或促癌的風(fēng)險降至最低�。相反�,生糖飲食可以大幅提高胰島素水平,促癌能力當(dāng)然有所提升了�。由此可見,胰島素抵抗及2型糖尿病患者的致癌風(fēng)險很高���。
生糖飲食為何提高致癌風(fēng)險?
不過��,究竟是高胰島素血癥還是高葡萄糖血癥促進腫瘤細胞生長尚無定論�,也許不同腫瘤及不同細胞有所差異。有人認為高糖環(huán)境可以通過多條途徑促進腫瘤進展�����。例如,高糖通過上調(diào)葡萄糖轉(zhuǎn)運蛋白GLUT1和GLUT3����、生長因子及其受體、其他生長促進信號�,可以加速腫瘤細胞增殖。高糖通過上調(diào)缺氧誘導(dǎo)因子����、脯氨酸水化酶和細胞色素c,也與腫瘤細胞的抗凋亡活性有關(guān)(參考文獻9)��。
我們也發(fā)現(xiàn)����,胰島素不僅不能促進腦垂體瘤細胞的生長及其腫瘤標志物的表達,反而抑制生長與表達���。倒是高濃度的葡萄糖卻促進腦垂體瘤細胞的快速增殖�����,并伴隨腫瘤標志物表達上調(diào)以及細胞凋亡率下降等現(xiàn)象(論文數(shù)據(jù)整理中)����。
兩點初步結(jié)論
鑒于腫瘤細胞具有線粒體功能缺陷的特點,限制葡萄糖供應(yīng)肯定不利于腫瘤的增殖和轉(zhuǎn)移���。作為化療或放療的輔助手段��,以生酮飲食為代表的代謝干預(yù)可能進一步加劇腫瘤細胞的死亡����。
不過��,體內(nèi)代謝狀況復(fù)雜�����,腫瘤細胞的生命力旺盛��,單純的生酮飲食可能不足以完全制服腫瘤惡變��,而且可能還表現(xiàn)組織�����、類型��、時期差異性���,如肝癌是否會得益于肝臟的糖異生作用��,也是今后需要深入研究的問題����。
參考文獻
1. Nebeling LC et al. 1995. Effects of a ketogenic diet on tumor metabolism and nutrational status in pediatric oncology patients: two case reports. J Am Coll Nutri 14: 202-208
2. Zhou W et al. 2007. The calorically restricted diet, an effective alternative therapy for malignant brain tumor. Nutr Metab (London) 4: 5
3. Zuccoli G et al. 2010. Metabolic management of glioblastoma multiforme using standard therapy with a restricted ketogenic diet: case report. Nutr Metab (London) 7: 33
4. Champe CE et al. 2014. Targeting metabolism with a ketogenic diet during the treatment of glioblastoma multiforme. J Neurooncol 117: 125-131
5. Gluschnaider U et al. 2014. Long-chain fatty acid analogues suppress breast tumorigenesis and progression. Cancer Res 74: 6991-7002
6. Masko EM et al. 2010. Low-carbohydrate diets and prostate cancer: how low is "low enough"? Cancer Prev Res (Phila) 3: 1124-1131
7.Shukla SK et al. 2014. Metabolism reprogramming induced by ketone bodies diminishes the pancreatic cancer cachexia. Cancer Metab 2: 18
8. Rieger J et al. 2014. ERGO: a pilot study of ketogenic diet in recurrent glioblastoma. Int J Oncol 44: 1843-1852
9. Ryu TY et al. 2014. Hyperglycemia as a risk factor for cancer progression. Diabetes Metab J 38: 330-336